Химия цвета.
Несколько слов о причинах окраски минералов.

Образец родохрозита «Королева Альмы». Sweet Home mine, США
Просто цвета не бывает.
Человек - существо, по природе своей очень любопытное. Особенно в раннем возрасте — все знают, что детей хлебом ни корми, дай только задать вопрос, ответ на который лежит в области квантовой электродинамики или теории струн. Взрослым порой приходится непросто, но на то они и взрослые — справляются как-то. Порой это выглядит довольно забавно — каких только странностей о нашем мире не наслушаешься от дошколят с безапелляционным: «Мне так папа/мама сказал/а!», звучащим после твоего законного недоумения. Но, к счастью, допрос родителей об устройстве и судьбах Вселенной продолжается всего года три-четыре, а потом не помощь приходит школа... Затем университет, колледж, училище и прочие типы образования, стремящиеся завершить картину мира у отдельно взятого человека. Но так или иначе люди продолжают задавать вопросы и в десять и в пятьдесят. Правда, с возрастом, волновать начинает уже курс доллара и номер автомобиля того нехорошего человека, который поцарапал вам бок, а не уравнения термоядерных реакций. Такова жизнь и это, каким бы странным ни казалось, прекрасно. Если бы все заботились о расшифровке генома мамонта и графене, то люди бы вымерли.
Но что если существуют невероятно простые вопросы, которые не задаются почти никогда? Каждый день мы задаем десятки вопросов, похожих на эти, даже с теми же словами, а эти, словно редкие снежные барсы, избегают встреч с человеком. И вот один из них: «Что такое цвет?».
«Как!» - скажете вы - «Я знаю, что такое цвет! Это синий, зеленый, красный — такое свойство объектов!» И вы ошибетесь. Потому что на самом деле — цвета, как такового, не существует. Взгляните на одно из словарных определений цвета: качественная субъективная характеристика электромагнитного излучения оптического диапазона, определяемая на основании возникающего физиологического зрительного ощущения и зависящая от ряда физических, физиологических и психологических факторов. Сколько оговорок, правда?
Говоря простыми словами — то, что мы называем цветом, не более чем ощущение.
Рассуждать об устройстве глаза (вы наверняка что-то сами читали об этом, а также про то, что у разных животных глаза устроены по-разному...) я не буду, рассмотрим его как черный ящик, принимающий отраженный свет, и потом отправляющий электрический импульс в мозг, этакий фотоэлемент. А интересовать нас сегодня будет то, что происходит на или в природном кристаллическом (или не очень) веществе. Итак, наш вопрос, звучащий очень и очень часто в определенных кругах: «Почему минералы именно такого цвета?»
Причины окраски по Ферсману. Первое приближение.
Известным геохимиком и минералогом А. Е. Ферсманом в начале прошлого века была предложена следующая классификация вариантов окрасок минералов, которая невероятно удобна, логична и понятна.
1. Идиохроматическая окраска — собственный цвет минерала, который зависит от его химической формулы, кристаллической структуры и ее особенностей (к примеру, дефектов).
2. Аллохроматическая окраска — окраска за счет примесей элементов-хромофоров (эдаких атомов-красок) или включений других минералов, пузырьков газа и т.д.
3. Псевдохроматическая окраска — окраска за счет исключительно физических причин. Сюда относятся радужные пленки побежалости, иризация, игра опалов и еще ряд явлений, которые отлично объясняются школьным курсом оптики (ключевые слова: дифракция, интерференция, полное внутреннее отражение).
К сожалению, физика псевдохроматических окрасок, где процессы похожи на большой теннис с мячиками, постоянно меняющими цвет, выходит за рамки этой статьи, а подробно мы остановимся на причинах идиохроматической и аллохроматической окрасок.
На уровень ниже — окраска за счет избирательного светопоглощения и все все все.
Чтобы действительно увидеть, как рождается свет, нам надо спуститься на уровень ниже и посетить кристаллическую структуру минерала и внимательно рассмотреть несколько странных атомов. Но это дело достаточно небезопасное без подготовки, поэтому давайте вспомним несколько вещей.
Итак. Собственно минералом называется природное кристаллическое вещество с неизменным химическим составом. Данному составу может соответствовать одна или более кристаллическая структура, но соответствовать должна обязательно («исторические» минералы, вроде опала и ртути не в счет).
Теперь об электромагнитном излучении: оно одновременно и частица и волна, поэтому говорить мы будем о фотонах, которые будут летать туда-сюда и обладать какой-либо длиной волны (эта-то характеристика и отвечает за цвет, который мы, в итоге, увидим). Собственно светом называется «видимый диапазон» электромагнитного излучения (длины волн 400-800 нанометров).
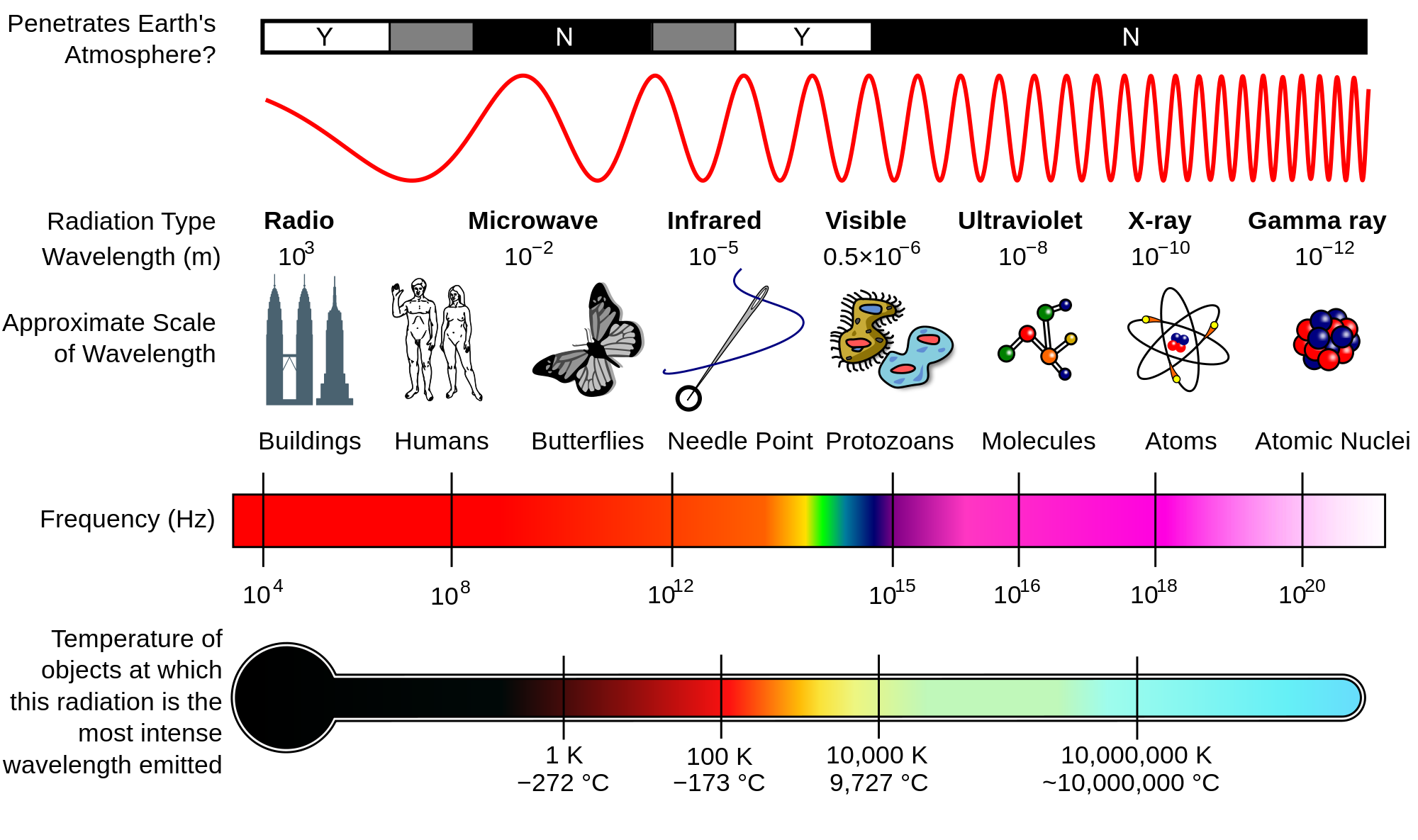
Спектр электромагнитного излучения и относительные размеры волн
Так получилось потому, что максимум интенсивности излучения нашей звезды приходится именно на этот промежуток, а наш глаз эволюционировал в непосредственной близости от нее.
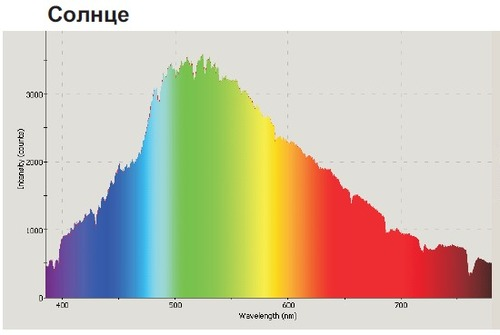
Спектр Солнца в видимой области в координатах длина волны/интенсивность излучения
Свет бывает белый (состоит из всех цветов сразу, из него удобно делать радуги), монохроматический (это когда все фотоны в пучке, с длинами волн соответствующими зеленому, к примеру, цвету) и какой попало (когда излучение, по сути, просто толпа разных фотонов). Природный свет именно такой — состоит из кучи разных волн с разными длинами.
Про атом: состоит из ядра и электронных уровней — стеллажа, на полках которого лежат электроны с разными значениями энергий. Ближе к ядру — с высокими энергиями, подальше от ядра — с низкими. Чтобы «переложить» электрон с верхней полки на нижнюю надо сообщить ему энергию, например, запустить по нему каким-нибудь фотоном. Энергия фотона зависит от его длины волны. Но для стабильности атома надо, чтобы на каждой полочке лежало ровно столько электронов, сколько надо, лишние там ни к чему. Поэтому несчастный «переложенный» электрон будет стремиться вернуться на свой родной уровень-полочку и испустить какой-нибудь фотон. Это, конечно, частный случай электронного перехода — есть и другие — но, надеюсь, что смысл ясен.
Итак: светопоглощение происходит за счет переходов электронов в структуре вещества из положения, стационарного (основного) для данной структуры и типа химической связи в ней, в вакантные (энергетически невыгодные), но все же потенциально возможные позиции. Это происходит за счет поглощения энергии света при его пропускании веществом или отражении. Соответственно, цвет характеризуется спектрами пропускания и отражения.
И вот тут возможны варианты...
1) Если величина Еп (энергия перехода электрона между уровнями) больше энергии света, электроны не будут переходить в другие позиции, свет не взаимодействует с веществом, не отдает ему энергии, оно оказывается прозрачным и бесцветным. Таковы алмазы, горный хрусталь и лед.

Флюорит. Clara Mine, Rankach valley, Oberwolfach, Wolfach, Black Forest, Baden-Württemberg, Germany
Оригинал: http://www.mindat.org/photo-641811.html
2) Значения Еп очень малы (< 0,5 эВ), что характерно для металлов с "электронным газом", осуществляющим химическую связь в них и допускающим легкое перемещение электронов. Все лучи света обладают достаточной энергией для "выбивания" электронов в вакантные позиции; поглощаются все лучи света, материя становится черной и непрозрачной (свет проходит на глубину не более 10^-8 м). По такой логике золото, серебро и платина должны были быть черными, а девушки были бы лишены удовольствия носить из них кольца. Но, к счастью модниц и африканских диктаторов, этот идеальный случай не реализуется и часть света все же отражается.

Медные «слои» в агате. Calumet & Hecla No. 21 mine, Calumet & Hecla Mine, Calumet, Calumet Township, Houghton Co., Michigan, USA
Оригинал: http://www.mindat.org/photo-681459.html

Золото. Eagle's Nest Mine, Placer Co., California, USA
Оригинал: http://www.mindat.org/photo-15167.html
3) Неравномерное поглощение света - причина цветовой окраски у прозрачных веществ-диэлектриков, в составе которых есть химические элементы-хромофоры (обычно, ионы переходных металлов периодической системы с номера 22 по 29, с 40 по 47 и выше; наиболее важные из них Тi, V, Сr, Мn, Fe, Со, Ni, Сu). Они обладают сложной конфигурацией электронных уровней, которая сильно подвержена влиянию соседей по материи. В результате — разные энергии переходов и излучения дают такой результат: оно окрашивается в цвет, дополнительный к поглощенному.
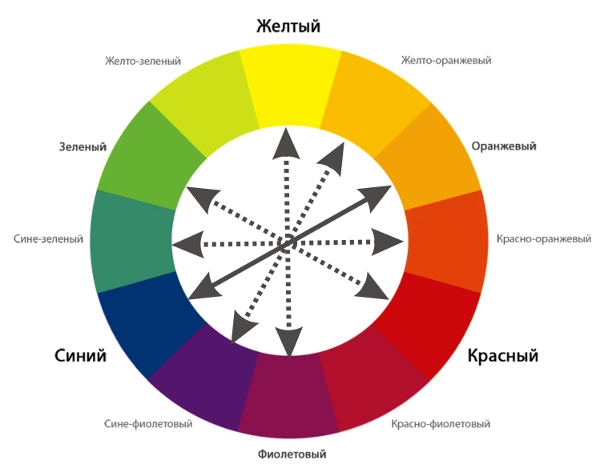
Таблица добавочных цветов
Это, наверное, самый распространенный случай, в минеральном мире. Вот несколько примеров: изумруд (окрашен хромом и ванадием), цитрин (железо), рубин (хром).
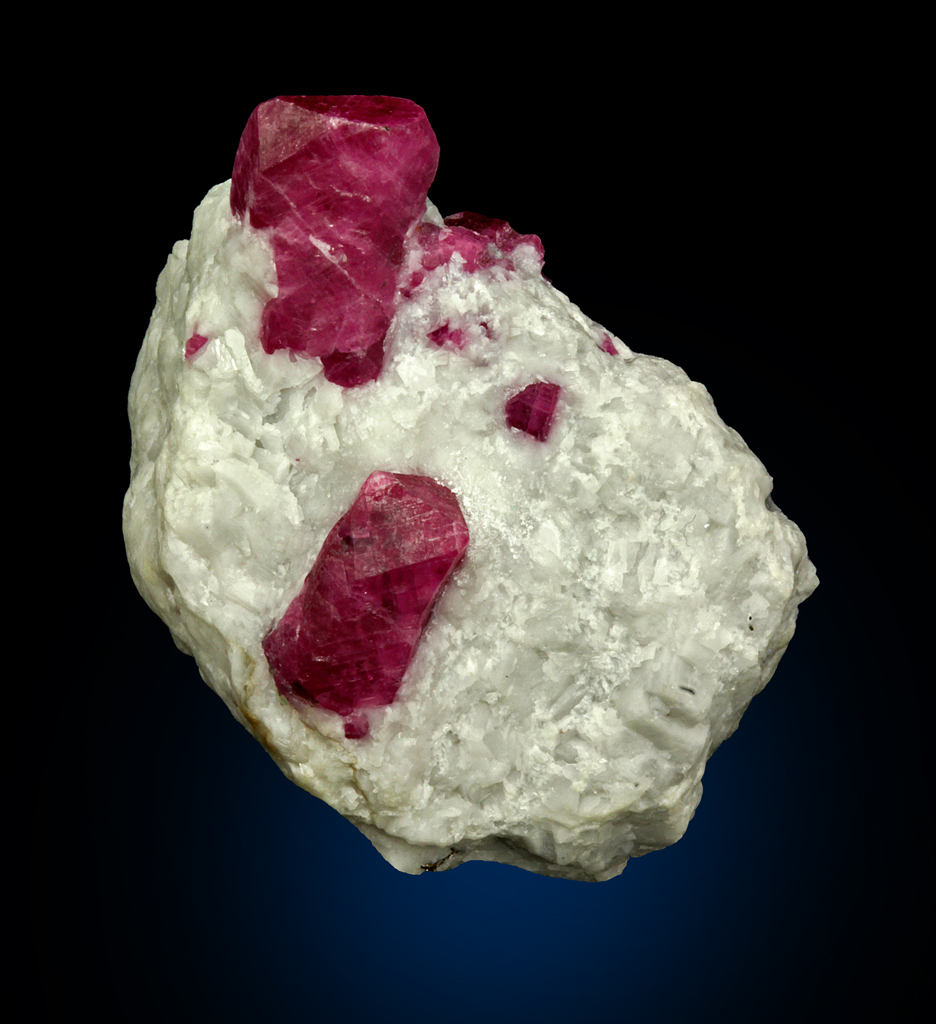
Рубин. Jegdalek ruby deposit, Surobi District, Kabol Province, Afghanistan
Оригинал: http://www.mindat.org/photo-327641.html

Изумруд. Muzo Mine, Mun. de Muzo, Vasquez-Yacopí Mining District, Boyacá Department, Colombia
Оригинал: http://www.mindat.org/photo-645211.html
4) Явление переноса заряда — при наличии комплексного иона, в нем может произойти смещение электрона от кислорода к металлу за счет поглощения энергии, равной как раз энергии какой либо части белого света.
Примеры: сапфир, крокоит (комплекс [CrO4].

Крокоит. Adelaide Mine, Dundas mineral field, Zeehan District, Tasmania, Australia
Оригинал: http://www.mindat.org/photo-145785.html

Сапфир. Ratnapura, Ratnapura District, Sabaragamuwa Province, Sri Lanka
Оригинал: http://www.mindat.org/photo-272893.html
5) Наличие в их кристаллической структуре электронно-дырочных центров окраски. Под действием света электрон «перескакивает» в дырку с поглощением части энергии.
Классическим примером является флюорит, разнообразные окраски которого преимущественно «дырочного» типа.
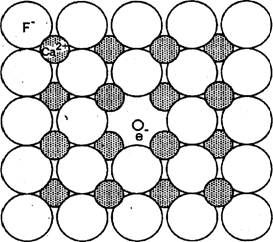
Перескок электрона в «дырку» во флюорите

Флюорит. Berbes, Berbes Mining area, Ribadesella, Asturias, Spain
Оригинал: http://www.mindat.org/photo-665665.html
Физика и химия цвета — невероятно увлекательная область науки. Хотя бы потому, что она дает потрясающую возможность правильно ответить ребенку на вопрос: «А почему трава зеленая?»
P.S. Потому что в траве хлорофилл, в хлорофилле железо, реализуется вариант 4.
Статья написана по материалам лекций, читавшихся на геохимическом потоке в рамках курса «Минералогия» и лекции на Летней Школе «Русского Репортера» в июле
2015 года.
Если у вас есть вопросы или замечания, касающиеся текста статьи, просьба написать мне на электронную почту: vlasov.k.94 «at» gmail.com (Власов Кирилл Алексеевич).
Другие статьи


